Nódulo tiroideo - ROSE
Nódulo tiroideo - ROSE
Por: Dra. Lina Marcela Restrepo Giraldo
Médica, Endocrinóloga, Laboratorio Clínico Hematológico S.A. Medellín, Colombia.
A pesar de que la prevalencia de nódulos tiroideos en la población general es alta (hasta de un 60% determinado por ecografía), muy pocos de ellos (alrededor del 5%) resultan malignos (1,2). El número creciente en el diagnóstico de nódulos tiroideos se puede atribuir, en gran medida, al uso cada vez más generalizado del diagnóstico por imágenes, el cual favorece la detección no solo de aquellos de tamaño pequeño sino de microcarcinomas papilares (2–4).
Estas consideraciones han planteado preocupación por los costos y la morbilidad potencial asociados con el manejo a corto y largo plazo de pacientes con nódulos tiroideos, que incluye visitas médicas periódicas, seguimiento ecográfico, estudios hormonales y aspirado para citología con aguja fina (ACAF), e incluso en algunos casos indeterminados, lobectomía tiroidea diagnóstica (1–4).
De esta manera, se requiere de un enfoque cuidadoso del tratamiento de estos nódulos tiroideos no malignos, al igual que para microcarcinomas con fenotipo de bajo riesgo, que pueden tratarse de forma segura mediante una cirugía más conservadora o incluso programas de vigilancia activa (3).
Los médicos que enfocan los pacientes con nódulos tiroideos deben evitar el sobrediagnóstico, sin poner en riesgo la posibilidad de identificar tumores de mayor riesgo que requieren un tratamiento específico. Además, la tamización activa de cáncer de tiroides no se recomienda en adultos asintomáticos sin factores de riesgo (1–4).
Evaluación inicial
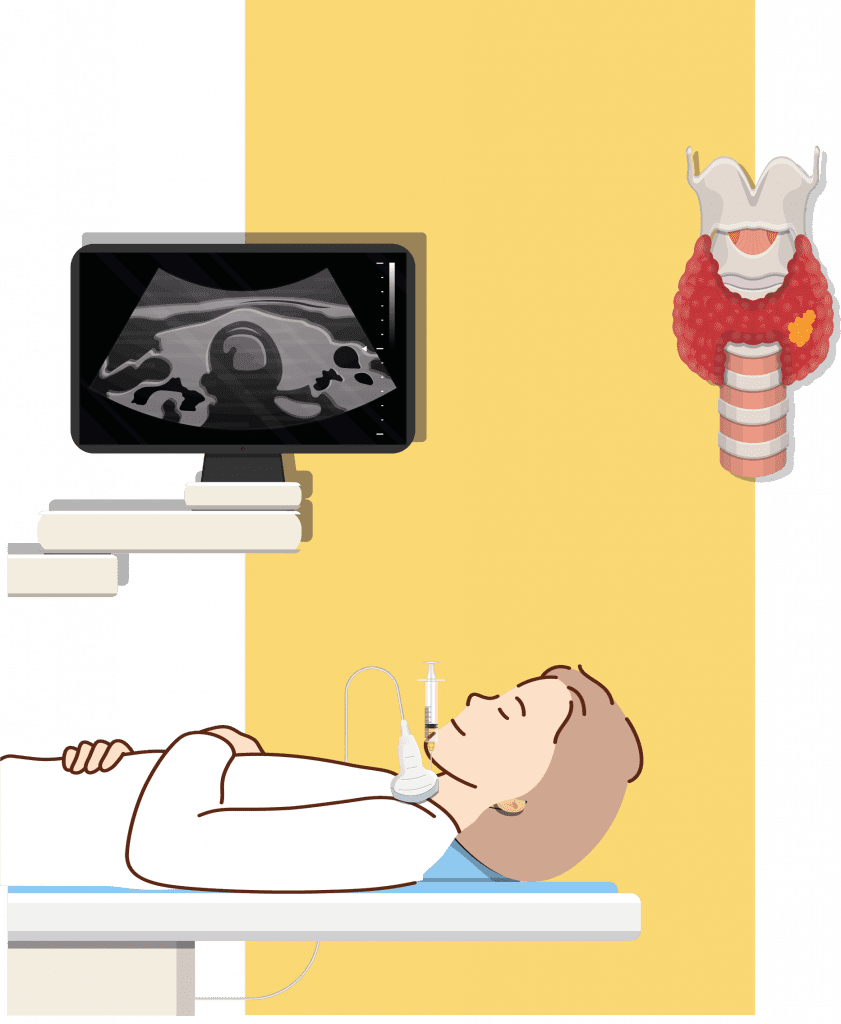
La evaluación inicial de un nódulo tiroideo clínicamente evidente o descubierto incidentalmente incluye la realización de ecografía y evaluación de los factores de riesgo clínicos. Dependiendo de los resultados, pueden requerirse herramientas de diagnóstico adicionales, como la punción y aspiración con aguja fina (ACAF) para citología, que estará indicada en un pequeño subconjunto de lesiones (2, 5–7).
La ecografía tiroidea es la herramienta de elección para la evaluación de la estructura de la tiroides. El exámen es seguro e indoloro y no requiere preparación. La ultrasonografía ayuda a la estimación inicial del riesgo de malignidad de los nódulos tiroideos según sus características ecográficas como (1, 3–5):
- Composición:si es sólida, quística o mixta.
- Forma: en este caso es importante definir si el nódulo es más ancho que alto o más alto que ancho.
- Márgenes: si son lisos, no definidos, lobulados o irregulares o con extensión extratiroidea.
- Presencia de calcificaciones u otros focos hiperecoicos.
- Características de todos los ganglios linfáticos cervicales.
Los hallazgos ecográficos consistentemente asociados con malignidad incluyen: hipoecogenicidad, márgenes irregulares o lobuladas, infiltración evidente, microcalcificaciones intranodulares y la forma más alta que ancha. Todas las ecografías deben incluir una exploración completa de todos los compartimentos de los ganglios linfáticos cervicales (6–8).
Con base en la información obtenida mediante ecografía tiroidea varias asociaciones académicas han desarrollado sistemas para la estratificación de riesgos de cáncer de tiroides:
- TI-RADS del Colegio Americano de Radiología 2017, con puntaje que define categorías por riesgos crecientes (8).
- Sistema de Clasificación de la Asociación Americana de Tiroides (ATA) 2016 (3).

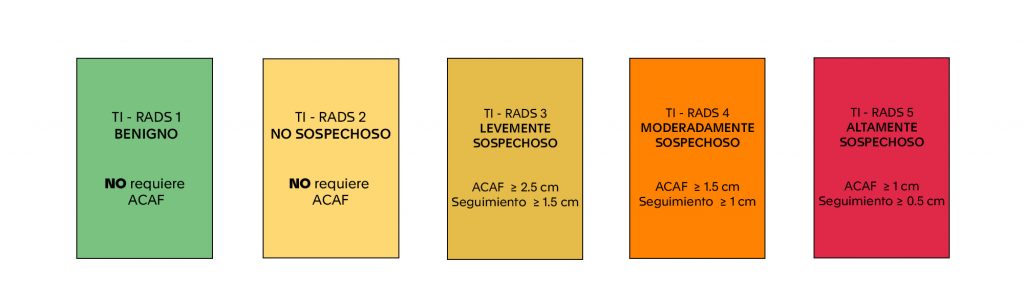
Figura 1: Puntaje TIRADS Colegio Americano de Radiología 2017.
Como ya se mencionó, algunos nódulos tiroideos requerirán un estudio que incluya citología con muestra tomada por ACAF (3). La evaluación rápida de la calidad de la muestra en el sitio de la punción (ROSE, del inglés Rapid On-Site Evaluation,) desempeña un papel importante que, más allá de proporcionar la certeza de haber obtenido material satisfactorio, va a permitir conocer un diagnóstico preliminar. Además, ayudar al operador a decidir si se requieren nuevas punciones con una orientación de la aguja de manera diferente, y a clasificar la muestra para definir si se necesitan pruebas adicionales o complementarias (9–11).
Con la inclusión de las pruebas moleculares para la evaluación de los nódulos tiroideos con hallazgos citológicos indeterminados, ROSE se está volviendo esencial para obtener una muestra adecuada. El Sistema Bethesda para el reporte de aspirados tiroideos recomienda el uso de ROSE cuando sea posible, especialmente cuando se hace el procedimiento después de muestras previas no diagnósticas (4,10,11).

Figura 2: Flujo de hallazgos mediante ecografía con ACAF más ROSE y evaluación citológica en la misma cita (12).
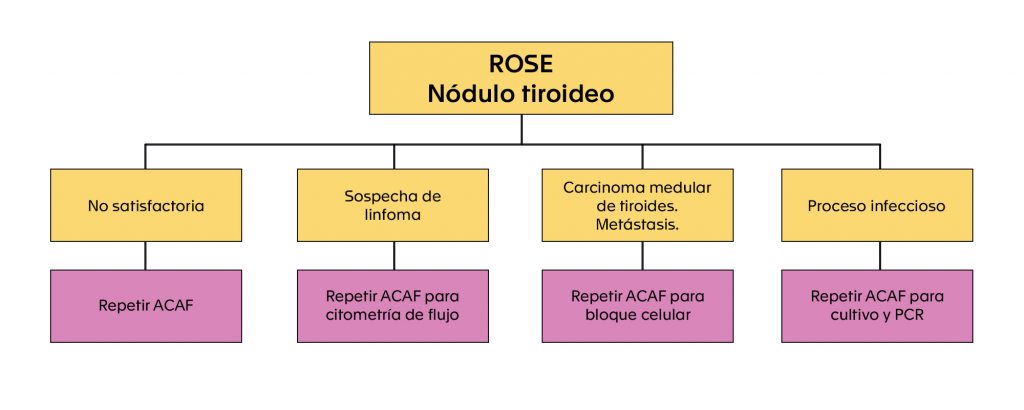
Figura 3. Flujograma de estudios complementarios según hallazgos en ROSE de nódulo tiroideo.
Laboratorio Clínico Hematológico
En el Laboratorio Clínico Hematológico estamos comprometidos con optimizar los tiempos de diagnóstico a favor de a comodidad del paciente, su tranquilidad y la oportunidad en la toma de decisiones diagnósticas y terapéuticas . Nuestro propósito es brindar el citodiagnóstico de un nódulo tiroideo en 48 horas o menos, en una única visita y con un muestreo satisfactorio. En circunstancias diferentes, debido a las dificultades en integrar la evaluación clínica, de imágenes y la citología, el paciente puede verse sometido a esperas de varios meses con múltiples visitas.
Bibliografía
- Grani G, Sponziello M, Pecce V, Ramundo V, Durante C. Contemporary Thyroid Nodule Evaluation and Management. J Clin Endocrinol Metab. 2020 Sep 1;105(9):2869–83. doi: 10.1210/clinem/dgaa322.
- Singaporewalla RM, Hwee J, Lang TU, Desai V. Clinico-pathological Correlation of Thyroid Nodule Ultrasound and Cytology Using the TIRADS and Bethesda Classifications. World J Surg. 2017 Jul;41(7):1807-1811. doi: 10.1007/s00268-017-3919-5.
- Burman KD, Wartofsky L. CLINICAL PRACTICE. Thyroid Nodules. N Engl J Med. 2015 Dec 10;373(24):2347-56. doi: 10.1056/NEJMcp1415786.
- Maxwell C, Sipos JA. Clinical Diagnostic Evaluation of Thyroid Nodules. Endocrinol Metab Clin North Am. 2019 Mar;48(1):61-84. doi: 10.1016/j.ecl.2018.11.001.
- Gharib H, Papini E, Garber JR, Duick DS, Harrell RM, Hegedüs L, Paschke R, Valcavi R, Vitti P; AACE/ACE/AME Task Force on Thyroid Nodules. american association of clinical endocrinologists, american college of endocrinology, and associazione medici endocrinologi medical guidelines for clinical practice for the diagnosis and management of thyroid nodules–2016 update. endocr pract. 2016 may;22(5):622-39. doi: 10.4158/ep161208.gl.
- Yang W, Fananapazir G, LaRoy J, Wilson M, Campbell MJ. can the american thyroid association, k-tirads and acr-tirads ultrasound classification systems be used to predict malignancy in bethesda category iv nodules? endocr pract. 2020 may 14. doi: 10.4158/ep-2020-0024. epub ahead of print.
- Vargas-Uricoechea H, Meza-Cabrera I, Herrera-Chaparro J. Concordance between the TIRADS ultrasound criteria and the BETHESDA cytology criteria on the nontoxic thyroid nodule. Thyroid Res. 2017 Feb 2;10:1. doi: 10.1186/s13044-017-0037-2.
- Koc AM, Adıbelli ZH, Erkul Z, Sahin Y, Dilek I. Comparison of diagnostic accuracy of ACR-TIRADS, American Thyroid Association (ATA), and EU-TIRADS guidelines in detecting thyroid malignancy. Eur J Radiol. 2020 Dec;133:109390. doi: 10.1016/j.ejrad.2020.109390.
- Jiang D, Zang Y, Jiang D, Zhang X, Zhao C. Value of rapid on-site evaluation for ultrasound-guided thyroid fine needle aspiration. J Int Med Res. 2019 Feb;47(2):626-634. doi: 10.1177/0300060518807060.
- Pastorello RG, Destefani C, Pinto PH, Credidio CH, Reis RX, Rodrigues TA, Toledo MC, De Brot L, Costa FA, do Nascimento AG, Pinto CAL, Saieg MA. The impact of rapid on-site evaluation on thyroid fine-needle aspiration biopsy: A 2-year cancer center institutional experience. Cancer Cytopathol. 2018 Oct;126(10):846-852. doi: 10.1002/cncy.22051.
- Tessler FN, Middleton WD, Grant EG, Hoang JK, Berland LL, Teefey SA, Cronan JJ, Beland MD, Desser TS, Frates MC, Hammers LW, Hamper UM, Langer JE, Reading CC, Scoutt LM, Stavros AT. ACR Thyroid Imaging, Reporting and Data System (TI-RADS): White Paper of the ACR TI-RADS Committee. J Am Coll Radiol. 2017 May;14(5):587-595. doi: 10.1016/j.jacr.2017.01.046.
- Michael CW, Kameyama K, Kitagawa W, Azar N. Rapid on-site evaluation (ROSE) for fine needle aspiration of thyroid: benefits, challenges and innovative solutions. Gland Surg. 2020 Oct;9(5):1708-1715. doi: 10.21037/gs-2019-catp-23.

